Ejemplo de Metalurgia
La Metalurgia es la ciencia de extraer los metales a partir de sus menas, así como la preparación de aleaciones, tratamiento térmico de metales, etcétera.
La Metalurgia de cada metal plantea un problema particular, cuya solución depende de sus propiedades químicas y de la naturaleza de las menas de las que se va a obtener. El problema es en parte Químico, y en parte Físico.
Las Menas son las piedras o minerales de donde se va a extraer el metal de interés. Las menas suelen tener concentraciones muy altas de este metal.
Contenido del artículo
Las Operaciones Metalúrgicas
Las Operaciones Metalúrgicas generalmente empleadas en la obtención de los metales pesados, como el hierro, el cobre, el Zinc, pueden dividirse en cuatro grupos:
Concentración
Algunas veces las menas, al extraerlas del suelo, contienen grandes cantidades de materias extrañas, como roca, arena, arcilla y caliza, que se conocen por el nombre genérico de Ganga. Con frecuencia conviene aplicar al principio un sencillo procedimiento mecánico para separar la mayor parte de la ganga, economizando así mucho combustible.
Este proceso se llama Concentración de la Mena. A veces se hace una tosca separación a mano, pero lo más corriente es reducir el mineral a partículas finas, separando la ganga de las partículas pesadas de la mena por medios puramente físicos, como agitación o cribado. En algunos casos, como sucede con las menas de cobre y de zinc (sulfuros), se aprovecha la humectación preferente de la mena para el aceite, y de la ganga para el agua (método de flotación).
El mineral se reduce a polvo muy fino, que se mezcla después con agua que contiene una pequeña cantidad de aceite de pino o aceite mineral y un producto espumante. Se hace luego burbujear aire a través de la suspensión, de modo que aparezca en la superficie en forma de espuma. El aceite moja la mena, que asciende a la superficie por la película oleosa que envuelve la burbuja de aire.
La ganga queda con el agua debajo de la espuma de aceite. Si el procedimiento se hace con cuidado, se podrá concentrar más del 90% del sulfuro en una décima parte del volumen inicial. Aquí se puede utilizar separación magnética, para eliminar Magnetita (Fe3O4) y chatarra.

Tostación
Después de concentradas, muchas menas se Tuestan. Esta operación consiste en calentar la sustancia finamente dividida en una corriente de aire o de gases de horno combinados con aire. Las menas sulfuradas se transforman en óxidos, separándose el azufre (S) y el arsénico (As) como óxidos volátiles, y los carbonatos (CO3-2) pasan a óxidos, por perder Dióxido de Carbono (CO2).
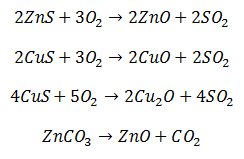
Reducción
La etapa siguiente es la Reducción, la que se efectúa en hornos especiales, donde la mena se mezcla con carbón, hulla o cok, y el monóxido de carbono producido por la combustión incompleta del carbón reduce el óxido a metal libre:
![]()
Al mismo tiempo, se añade un Fundente que se combina con la ganga para formar una Escoria Fusible, que flota sobre el metal fundido y lo preserva de la oxidación. Cuando la ganga es arena o material silíceo, el fundente es caliza:
![]()
Si el metal obtenido es volátil se extrae en forma de vapor y se recoge por Condensación. La mena de óxido o de sulfuro oxidado se mezcla con carbón y se calienta en una retorta. A la temperatura de la reacción, el metal es un vapor y pasa a condensadores especiales, donde queda como metal fundido. Tal sucede en la práctica con el zinc.
Algunos metales no se obtienen fácilmente reduciendo sus óxidos con carbón. El Aluminio (Al) es un reductor más enérgico, pero también más caro que el carbón.
Afinación
Finalmente, el metal en bruto obtenido por reducción hay que purificarlo. Tal como sale de los hornos, contiene impurezas, tal como pequeñas cantidades de escoria, gases disueltos, óxidos y sulfuros no reducidos y otros metales. El proceso de Purificación o Afinación, varía según la naturaleza del metal. El zinc y el mercurio, metales volátiles, se afinan por Destilación. Los metales de punto de Fusión bajo, como el Plomo y el Estaño, se separan de las impurezas fundiéndolos de nuevo con un fundente adecuado.
Muchos metales se afinan Electrolíticamente. El metal impuro constituye el ánodo, el electrolito es una disolución de una sal del metal, y empleando la tensión o voltaje apropiado, el metal deseado se deposita muy puro en el cátodo, quedando las impurezas en la disolución o como un sedimento sólido, barro anódico, en el fondo de la cuba. Casi todo el cobre que se consume en la industria se afina por electrólisis.
Otros Métodos Metalúrgicos
Cuando un metal, en este caso el Oro (Au), se encuentra en estado nativo, la mena finamente triturada se pone en contacto con mercurio. Las partículas de oro se disuelven en él, formando una amalgama de la que se recupera el oro separando por Destilación el mercurio. Este procedimiento se llama Amalgamación.

Cuando la concentración del metal en la mena es demasiado baja para reducirlo económicamente en un horno, la mena puede tratarse con disoluciones de reactivos químicos, como cianuro sódico o ácidos, que disuelven el metal. Este proceso se denomina Lixiviación. El metal puede obtenerse por precipitación con cinc o hierro (para el oro y la plata) o por electrólisis (para el Cobre).

Las Aleaciones
Cuando se mezclan dos o más metales en estado fundido y se deja solidificar, el producto se llama Aleación. Si uno de los componentes es el mercurio, la aleación recibe el nombre de Amalgama. En la mayoría de los casos, los metales son completamente miscibles entre sí en estado liquido, excepto el plomo y el zinc, pero al enfriar y solidificarse, el producto presenta a veces un aspecto heterogéneo.

Se observan en las aleaciones tres condiciones primarias:
1.- Los componentes cristalizan por separado, de manera que la aleación es un conglomerado de cristales de los componentes puros.
2.- Los metales permanecen completamente disueltos uno en otro, en estado sólido, constituyendo una solución sólida, o cristales mixtos. Las aleaciones de plata y oro muestran esta condición.
3.- Los componentes metálicos forman compuestos definidos y resulta una aleación homogénea. Así se conocen compuestos como Zn3Ag2, AlCu, NiBi, CuMg.
Cuando hay más de dos metales en una aleación, la estructura es a menudo muy compleja. El estudio de la estructura de las aleaciones constituye el objeto de una sección separada de la química, llamada Metalografía.
Ejemplos de Aleaciones Metalúrgicas:
Bronce de Aluminio, con 90% Cobre y 10% Aluminio.
Bronce de Cañón, con 90% Cobre y 10% Estaño.
Bronce de Manganeso, con 90% Cobre, 5% Zinc, 3% Estaño, 2% Manganeso.
Constantan, con 60% Cobre y 40% Niquel.
Duraluminio, con 95.5% Aluminio, 3% Cobre, 1% Manganeso, 0.5% Magnesio.
Latón amarillo, con 67% Cobre y 33% Zinc.
Latón rojo, con 90% Cobre, 10% Zinc.
Magnalium, con 90% Aluminio, 10% Magnesio.
Metal Babbitt, con 90% Estaño, 7% Antimonio, 3% Cobre.
Metal Britania, con 90% Estaño, 8% Antimonio, 2% Cobre.
Metal de campanas, con 78% Cobre, 22% Estaño.
Metal de espejos, con 67% Cobre, 33% Estaño.
¿Cómo citar? Contreras, V. & Del Moral, M. (s.f.). Ejemplo de Metalurgia.Ejemplo de. Recuperado el 26 de Septiembre de 2023 de https://www.ejemplode.com/38-quimica/4734-ejemplo_de_metalurgia.html
