Ejemplo de Compuestos Aromáticos
Los químicos han considerado útil dividir todos los compuestos orgánicos en dos grandes clases: compuestos Alifáticos y compuestos Aromáticos. Los compuestos Aromáticos son el Benceno y los compuestos de comportamiento químico similar. Las propiedades aromáticas son las que distinguen al Benceno de los Hidrocarburos Alifáticos. La molécula bencénica es un anillo de un tipo particular. Hay otros compuestos, también anulares, que parecen diferir estructuralmente del benceno y sin embargo se comportan de forma similar.
Resulta que estos otros compuestos se parecen al benceno en su estructura electrónica básica, por lo que también llegan a comportarse como aromáticos.
Los hidrocarburos alifáticos (alcanos, alquenos, alquinos y sus análogos cíclicos) reaccionan principalmente por adición, en los enlaces múltiples, y por sustitución por radicales libres, en otros puntos de la cadena alifática.
En cambio, los hidrocarburos aromáticos, se destaca que tienen la tendencia a la sustitución heterolítica. Además, estas mismas reacciones de sustitución son características de anillos aromáticos dondequiera que aparezcan, independientemente de los otros grupos funcionales que la molécula pudiera contener. Estos últimos grupos afectan a la reactividad de los anillos aromáticos, y viceversa.
Contenido del artículo
La molécula del Benceno
El benceno es conocido desde 1825, y sus propiedades químicas y físicas son mejor conocidas que las de ningún otro compuesto orgánico. A pesar de ello, hasta 1931 no se había logrado proponer una estructura satisfactoria para esta sustancia, y debieron transcurrir hasta 15 años para que fuera de uso general entre los Químicos orgánicos. La dificultad radicaba en las limitaciones del desarrollo que había alcanzado para entonces la teoría estructural. Se ha llegado a la estructura final gracias a que se asumen varios importantes hechos:
El Benceno tiene la fórmula molecular C6H6. Por su composición elemental y peso molecular, se sabía que el benceno tiene seis átomos de Carbono y seis de Hidrógeno. El problema era conocer la disposición de tales átomos.
En 1858, August Kekulé propuso que los átomos de Carbono se pueden unir entre sí para formar cadenas. Después, en 1865, ofreció una respuesta al problema del Benceno: estas cadenas carbonatadas a veces pueden ser cerradas, para formar anillos.
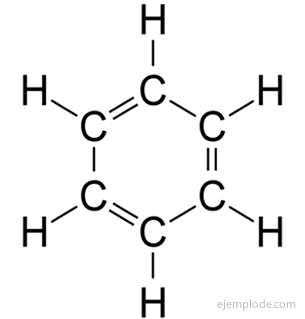
El Benceno sólo da un producto monosustituido C6H5Y. Por ejemplo, cuando se reemplaza un átomo de hidrógeno por Bromo, sólo se obtiene una única configuración de BromoBenceno C6H5Br; análogamente, también se obtiene un CloroBenceno C6H5Cl, o un NitroBenceno C6H5NO2, etc. Este hecho impone una severa limitación a la estructura del Benceno: todos sus Hidrógenos deben ser exactamente equivalentes, es decir, deben estar todos unidos a Carbonos que a su vez estén todos igualmente vinculados. No puede haber Hidrógenos en CH3, y otros en CH2, y otros en CH. La estructura final del monosustituido deberá ser la misma para la sustitución de cualquier Hidrógeno del Benceno.
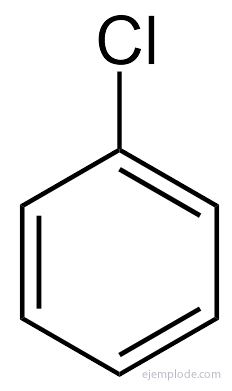
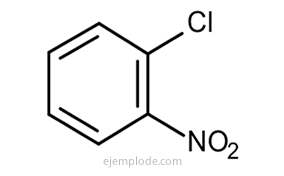
El Benceno da tres productos disustituidos isómeros, C6H4Y2 o C6H4YZ. Sólo existen tres DiBromoBencenos isómeros, C6H4Br2, tres CloroNitroBencenos C6H4ClNO2, etc. Este hecho limita aún más las posibilidades estructurales.
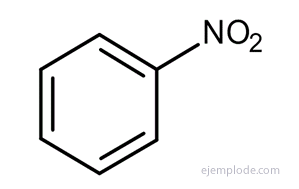
El Benceno experimenta reacciones de sustitución, más que de adición. La estructura bencénica de Kekulé corresponde a una que llamaríamos Ciclohexatrieno. Por esto, debería reaccionar con facilidad por adición, como lo hacen los compuestos similares, ciclohexadieno y ciclohexeno, que es una característica de la estructura de los alquenos. Pero ese no es el caso; en condiciones donde los alquenos reaccionan rápidamente, el benceno no reacciona, o sólo lo hace muy lentamente. En lugar de las reacciones de adición, el benceno experimenta con facilidad un conjunto de reacciones, todas de sustitución, como la Nitración, la Sulfonación, la Halogenación, la Alquilación de Friedel-Crafts, la Acilación de Friedel-Crafts. En cada una de estas reacciones, se ha sustituido un átomo o grupo, por uno de los átomos de Hidrógeno del Benceno.
La estabilidad del Benceno es debida a los enlaces dobles alternados y además a la energía de resonancia, en la que los dobles enlaces cambian de posición entre los carbonos, manteniendo la misma alternancia estructural. Esta energía de estabilización de resonancia es la responsable del conjunto de propiedades llamadas Propiedades Aromáticas.
Una reacción de Adición convierte a un alqueno en un compuesto saturado más estable. Pero en el caso del Benceno, una Adición lo vuelve menos estable por la destrucción del sistema anular sostenido y estabilizado por la resonancia. La molécula final sería el Ciclohexadieno. Es por ese hecho que la estabilidad del Benceno lo lleva a sólo reacciones de Sustitución.
Propiedades de los Compuestos Aromáticos
Además de las sustancias que contienen anillos bencénicos, hay muchas otras que se consideran aromáticas, a pesar de que superficialmente casi no guardan semejanza con el Benceno.
Desde el punto de vista experimental, los compuestos aromáticos son sustancias cuyas fórmulas moleculares hacen suponer un alto grado de insaturación, a pesar del cual son resistentes a las reacciones de adición tan características de los compuestos no saturados.
En cambio, estos compuestos aromáticos a menudo sufren reacciones de sustitución electrofílica similares a las del Benceno. Junto con esta resistencia a la adición, y probablemente a causa de ella, se encuentran pruebas de una estabilidad inusual, como bajos calores de hidrogenación y combustión.
Las sustancias aromáticas son cíclicas, por lo general presentando anillos de cinco, seis y siete átomos, y su examen físico demuestra que tienen moléculas planas o casi planas. Sus protones tienen el mismo tipo de desplazamiento químico en los espectros de Resonancia Magnética Nuclear que en los del Benceno y sus Derivados.
Desde un punto de vista teórico, para que una sustancia sea aromática, su molécula debe tener nubes cíclicas de electrones π deslocalizados encima y debajo del plano de la molécula; además, estas nubes π deben contener un total de (4n+2) electrones π; esto significa que no basta la deslocalización para que resulte la estabilidad particular que caracteriza a un compuesto aromático.
Nomenclatura de los Derivados del Benceno (Compuestos Aromáticos)
En el caso de muchos de estos derivados, sobre todo en los monosustituidos, basta con anteponer el nombre del grupo sustituyente a la palabra Benceno, como, por ejemplo, CloroBenceno, BromoBenceno, YodoBenceno, NitroBenceno.
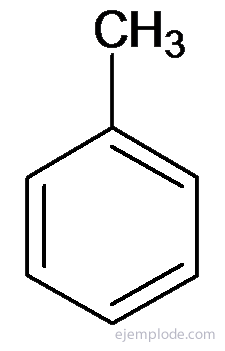
Otros derivados tienen nombres especiales que pueden carecer de semejanza con el nombre del grupo sustituyente. Por ejemplo, el MetilBenceno sólo se conoce como Tolueno; el AminoBenceno como Anilina; el HidroxiBenceno como Fenol, etc.
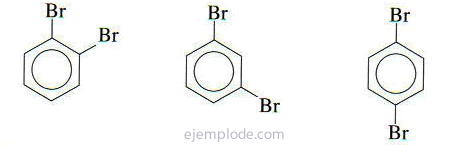
Si existen dos grupos unidos al anillo bencénico, no sólo es necesario identificar cuáles son, sino también indicar su ubicación relativa. Los tres isómeros posibles para bencenos disustituidos se caracterizan por los prefijos orto, meta y para, abreviados o-, m-, p-. Por ejemplo: o-DiBromoBenceno, m-DiBromoBenceno, p-DiBromoBenceno.
Si uno de los dos grupos es del tipo que da a la molécula un nombre especial, el compuesto se denomina como un derivado de aquella sustancia especial. Por ejemplo: NitroTolueno, BromoFenol, etc.
Ejemplos de Compuestos Aromáticos
Tolueno o MetilBenceno
EtilBenceno
IsopropilBenceno
TriNitroTolueno o TNT
Anilina o AminoBenceno
Ácido Benzoico
Ácido Glutámico o Ácido ParaAminoBenzoico
Ácido ToluenoSulfónico
Fenol o HidroxiBenceno
BromoFenol
TriCloroBenceno
Éter Fenil Bencénico
IodoBenceno
BromoBenceno
¿Cómo citar? Contreras, V. & Del Moral, M. (s.f.). Ejemplo de Compuestos Aromáticos.Ejemplo de. Recuperado el 26 de Septiembre de 2023 de https://www.ejemplode.com/38-quimica/4517-ejemplo_de_compuestos_aromaticos.html
