Ejemplos de Alquenos
Los Alquenos son compuestos orgánicos constituidos de Carbono e Hidrógeno dispuestos en cadena lineal o ramificada, con la presencia de al menos un enlace doble entre átomos de Carbono. También reciben el nombre de Hidrocarburos Alifáticos Insaturados u Olefinas.
El enlace doble que caracteriza este tipo de molécula está formado por un enlace sigma (σ) y un enlace pi (π). El enlace sigma es conocido como el enlace covalente más fuerte que involucra a los dos átomos, en su valencia directa contenida en el orbital s. Se asume como el enlace principal. El enlace pi es el enlace suplementario, que se forma entre los orbitales p de los átomos.
Dada su fórmula general CnH2n, se conoce que la presencia de átomos de Hidrógeno es el doble de la de átomos de Carbono en la molécula. El compuesto más simple de la Serie es el Etileno o Eteno, C2H4, y le aporta otro nombre a la serie de los Alquenos: Etilenos.
La capacidad de estos compuestos de reaccionar es mayor que en los Alcanos. Con la presencia del enlace doble, los átomos no están tan fuertemente ligados, y en la sencilla ruptura del enlace pi, ocurre una sustitución por un átomo, que abarcará esa libertad de enlace. Dicho átomo nuevo puede ser un Halógeno (Cloro, Bromo, Iodo), un Hidrógeno, un Metal o un No metal.
Propiedades como la Densidad, Viscosidad, y los puntos de Ebullición y Fusión, aumentan si el número de átomos de Carbono es mayor. Su solubilidad en Agua sigue siendo nula, al no tener la Polaridad necesaria. Sólo son solubles en solventes no polares, como el Hexano.
Los alquenos más sencillos, el Eteno, Propeno y Buteno, son gases. Los siguientes, de cinco a quince átomos de carbono son líquidos, y de dieciséis en adelante se manifiestan en estado sólido a temperatura ambiente, estandarizada a 25°C.
Contenido del artículo
Estructura y Nomenclatura de los Alquenos
Los Alquenos se nombran, primero, tomando en cuenta la cadena más larga de Carbonos. El requisito para esto es poner atención al extremo al que esté más próximo el enlace doble; éste tendrá la prioridad. Se nombrarán las ramificaciones, y al final el alqueno, porque es el dominio en que se está trabajando. Habrá veces en que la molécula tendrá dos o más enlaces dobles. Se nombra tomando en cuenta el que esté más próximo a un extremo de la cadena, y al alqueno se le colocará un prefijo numérico “di”, “tri”, etc.
Por ejemplo:
![]()
La cadena más larga es de cuatro carbonos, lineal y sin ramificaciones. Hay dos enlaces dobles, ambos en posiciones simétricas: 1 y 3. Al ser un buteno, se llamará 1,3-butadieno, agregando ya el prefijo “di” por la presencia de 2 enlaces dobles.
Siguiente ejemplo:
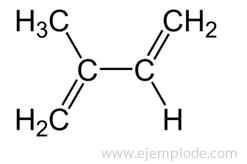
Para el compuesto de la imagen, la cadena más larga donde existen todos los enlaces dobles es de 4 Carbonos. Ambos enlaces dobles están simétricos en la cadena, así que daría igual por dónde comenzamos a nombrar. Sin embargo, tenemos presente un grupo Metil en la segunda posición de la izquierda. Por ahí comenzaremos: 2-metil-1,3-butadieno o Isopreno, que es el nombre comercial de este compuesto.
Siguiente ejemplo:
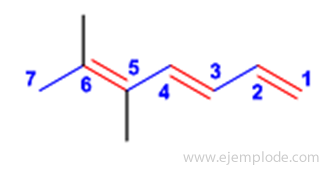
Están señalados tres enlaces dobles. Uno de ellos está en un extremo, por lo que los átomos de Carbono se nombrarán a partir de ahí. Hay también dos ramificaciones hechas de Radicales Metil. Las posiciones de los enlaces dobles son 1,3,5. Y las posiciones de las ramificaciones son 5 y 6. El nombre del compuesto será: 5,6-Dimetil-1,3,5-Heptatrieno.
Aplicaciones de los Alquenos
Los primeros alquenos de la serie, el Etileno y el Propileno, de dos y tres Carbonos respectivamente, se utilizan como precursores de dos de los polímeros más importantes en la industria: los plásticos Polietileno de baja y alta densidad, y Polipropileno.
El 2-metil-1,3-Butadieno, o Isopreno se encarga de la constitución del Caucho natural, como una goma o plástico negro del que se fabrican las llantas para toda categoría de vehículos.
Polietileno
Es el polímero más simple, con una estructura básica de (-CH2-CH2-)n, tiene propiedades similares a las de un alcano de alto peso molecular. Tiene una apariencia de película entre transparente y translúcida. Se utiliza para bolsas plásticas de supermercado, cubiertas para cableado, envolturas. Se clasifica en dos tipos de acuerdo con su estructura: Polietileno de Alta Densidad (HDPE), que consta de cadenas lineales ordenadas, y Polietileno de Baja Densidad (LDPE), constituido de cadenas enramadas, de las que caben menos por unidad de volumen.


Aplicaciones del Polietileno
Polipropileno
Está compuesto por unidades de Propileno, que generan un plástico más resistente que el Polietileno. Se utiliza frecuentemente en recipientes para detergentes, para contenedores, estuches, sobres plásticos para proteger documentos, pastas para engargolado, materiales para laboratorio como probetas y embudos, taparroscas para envases de bebidas; en fin, sus aplicaciones son muy diversas.
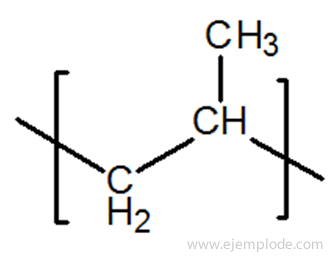
Unidad de Propileno, principal componente del Polipropileno


Aplicaciones del Polipropileno
Poliisopreno o Caucho
Tiene como base la estructura del Isopreno, mencionado anteriormente. El caucho es un hidrocarburo de gran importancia, que se obtiene del látex de ciertos árboles de la zona tropical. Cuando se calienta el látex, o se le añade ácido acético, los hidrocarburos en suspensión, con pequeñas cantidades de otras sustancias, se coagulan y pueden extraerse del líquido. El producto obtenido es el caucho bruto del comercio, viscoso y pegajoso, blando en caliente y duro y quebradizo en frío. Al estirarlo, no vuelve a adquirir después la forma primitiva (no es elástico).
En 1839, Charlie Goodyear descubrió que amasando bien el caucho con azufre y calentándolo a una temperatura superior a 100°C, el azufre se combina químicamente con el caucho y el producto que resulta tiene propiedades mucho más útiles. No se deforma con el calor, no es quebradizo en frío y no es pegajoso. Además, es medianamente elástico.
Anillos de S8 se abren y se combinan con los dobles enlaces de las moléculas de poliisopreno formando puentes de cadenas de azufre de una molécula de caucho a otra, y dando lugar a una trama total. Este proceso se llama Vulcanización. Para acelerar la vulcanización, actúan sustancias como negro de humo, óxidos de zinc y plomo, y muchos productos orgánicos.
 Extracción del látex del árbol de la zona tropical
Extracción del látex del árbol de la zona tropical
 Caucho en diferentes granulometrías
Caucho en diferentes granulometrías
 Producto terminado: Neumáticos
Producto terminado: Neumáticos
¿Cómo citar? Contreras, V. & Del Moral, M. (s.f.). Ejemplos de Alquenos.Ejemplo de. Recuperado el 12 de Noviembre de 2025 de https://www.ejemplode.com/38-quimica/4494-ejemplo_de_alquenos.html
