Ejemplo de Química Orgánica
La Química Orgánica es la parte de la Química General encargada del estudio y la clasificación funcional de los compuestos químicos cuyo elemento estructural es el Carbono, presente en abundancia en la materia viva; así se crea un universo bien diferenciado de la Química Inorgánica, dedicada a los compuestos químicos catalogados como minerales.
El átomo de Carbono tiene cuatro electrones en la última capa de su configuración electrónica. Esta característica, junto con la de su radio atómico, le permite unirse mediante enlaces covalentes a otros átomos del mismo elemento, en cadenas numerosas, formando una gran diversidad de compuestos químicos estables.
Puedes consultar Enlaces covalentes.
Tales compuestos químicos, además de los átomos de Carbono que les brindan la estructura primordial, contienen átomos de Hidrógeno como complemento principal para la valencia del Carbono. Además, en esta diversidad de compuestos, existen aquellos con intervención de átomos de Oxígeno, Nitrógeno, Halógenos, Azufre e incluso Fósforo, elementos alcalinos y alcalinotérreos y metales de transición. Dependiendo de los que se involucren en la molécula, serán las propiedades físicas y químicas de la sustancia final.
Los compuestos orgánicos están presentes en toda la materia viva; propician y sustentan todas las funciones biológicas, al contrario de las sustancias inorgánicas o minerales, que han sido utilizadas por el ser humano con fines comerciales, de experimentación o para cumplir con ciertas tareas domésticas.
Contenido del artículo
Historia de la Química Orgánica
Para antes de 1828, ya se hacía la distinción entre Química Orgánica y Química Inorgánica. A la materia orgánica se le asociaba con una creación a través de una “fuerza vital”, y a la inorgánica con lo no vivo, con lo mineral. Dadas estas concepciones, no se podía esperar obtener en laboratorio compuestos orgánicos a partir de materiales inorgánicos.
Sin embargo, en 1828 Friedrich Wöhler (1800-1882) consiguió preparar una sustancia orgánica, la Urea CO(NH2)2, producto importante del metabolismo animal, a partir de compuestos inorgánicos. Trató Cianato de Plomo Pb(CNO)2 con Amoníaco NH3 para obtener Cianato de Amonio NH4CNO; se formó este compuesto, efectivamente, pero al hervir la disolución para cristalizar el Cianato de Amonio, éste se transformó en Urea.
Este cambio químico es un ejemplo de Reagrupamiento interno, en el cual no cambia el número ni la clase de los átomos en la molécula, sino solamente su orden dentro de la misma. Este tipo de transformaciones son muy corrientes en química orgánica.
El descubrimiento de Wöhler inició el abandono de la teoría de la fuerza vital, más tarde completamente desechada al ser seguido por la preparación de otros muchos compuestos orgánicos en el laboratorio. A pesar de ello, subsisten los calificativos de Inorgánico y Orgánico, ya que los compuestos inorgánicos se relacionan con los productos minerales y los compuestos orgánicos, que son en realidad compuestos de carbono e hidrógeno y sus derivados, son del tipo producido por los organismos vivos.
Aunque las leyes de la química general se aplican por igual a unos y otros compuestos, diversas causas justifican y hacen necesaria esta división. Así, los compuestos orgánicos e inorgánicos se diferencian en distintas propiedades, como son: su Solubilidad preferente en disolventes orgánicos (éter, alcohol, cloroformo, etc) y en agua, respectivamente, su Estabilidad (los compuestos orgánicos se descomponen a temperaturas relativamente bajas), y el Carácter de las Reacciones; para los compuestos inorgánicos son iónicas, sencillas y prácticamente instantáneas, y para los compuestos orgánicos son covalentes, complejas y lentas.
Los compuestos orgánicos
Del Carbono se conocen compuestos de cadenas hasta de noventa átomos. Las cadenas de átomos de Carbono pueden ser lineales y ramificadas y tener simples enlaces covalentes o presentar dobles o triples enlaces. Se conocen más de 2,500 compuestos que contienen únicamente Carbono e Hidrógeno (Hidrocarburos).
Isomería de los compuestos orgánicos
En los compuestos inorgánicos, una fórmula representa por lo general un solo compuesto; así, únicamente existe una substancia de fórmula H2SO4. La molécula del Ácido Sulfúrico contiene dos átomos de Hidrógeno, uno de Azufre y cuatro de Oxígeno, en una ordenación determinada y única. En los compuestos orgánicos es poco frecuente que esto pase. Así, por ejemplo, hay dos compuestos que responden a la fórmula C2H6O, el Alcohol etílico o Etanol, y el Eter dimetílico.

Cuanto más compleja es la molécula, esto es, cuanto mayor sea el número de átomos de Carbono, tanto mayor es el número de isómeros posibles.
Análisis de los Compuestos Orgánicos
El análisis de un compuesto orgánico comprende el análisis cualitativo, el análisis cuantitativo y el análisis funcional. En el caso de suponerse que se encuentra el compuesto en estado impuro, se purifica previamente mediante Cristalización, Destilación, Sublimación, Extracción, etc. El criterio de pureza puede juzgarse según sus constantes físicas, como el punto de fusión, el punto de ebullición, densidad, solubilidad, forma cristalina, índice de refracción, etc.
El análisis cualitativo se verifica investigando la presencia de los elementos que constituyen el compuesto, especialmente del Carbono, el Hidrógeno y el Nitrógeno, y en ocasiones los Halógenos, Azufre y Fósforo.
El análisis cuantitativo se lleva a cabo utilizando como base los métodos empleados para el análisis cualitativo. Se parte de una cantidad determinada de sustancia que se somete a combustión, y se recoge y pesa el dióxido de carbono y el vapor de agua formados para el cálculo del tanto por ciento de Carbono e Hidrógeno en el compuesto. Los resultados del análisis cuantitativo facilitan el cálculo de la fórmula empírica, si bien la fórmula molecular sólo podrá encontrarse después de la determinación del peso molecular de la sustancia. Pero el problema no queda aún resuelto, porque la misma fórmula molecular puede corresponder a diferentes isómeros.
Clasificación de los Compuestos Orgánicos
De acuerdo con su estructura, los compuestos orgánicos se dividen en compuestos alifáticos, aromáticos y heterocíclicos. Los compuestos alifáticos están relacionados con el metano CH4, son de cadena abierta, excepto las cicloparafinas, y deben su nombre al hecho de que las grasas animales y vegetales pertenecen a este grupo.
Los compuestos aromáticos, de cadena cerrada, guardan estrecha relación con el benceno, C6H6, y deben su nombre a que muchos de ellos tienen olores fragantes, agradables.
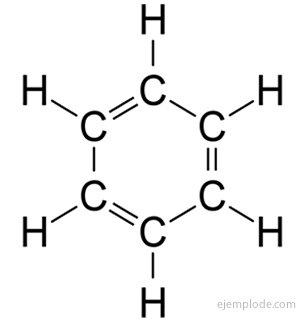
Anillo de Benceno
Los compuestos heterocíclicos son compuestos de cadena cerrada en cuyo anillo hay algún elemento distinto al carbono.
Por su constitución, se encuentran:
Hidrocarburos, que a su vez, por el tipo de enlaces que posee, se clasifica en Alcanos, Alquenos y Alquinos. Además, se encuentran en esta categoría los Cicloalcanos, el Benceno y sus derivados únicamente constituidos por Carbono e Hidrógeno.
Compuestos heterocíclicos
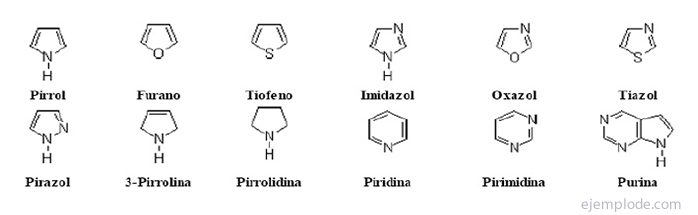
Derivados Halogenados: R-X
Nitrocompuestos: R-NO2
Ácidos Sulfónicos: R-SO3H
Nitrilos (O cianuros de alquilo) e Isonitrilos: R-CN y R-NC. Difieren en cómo está enlazado el átomo de Nitrógeno en la molécula.
Alcoholes: R-OH
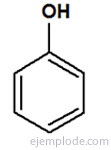
Fenoles: Compuestos basados en una estructura principal que consiste de un anillo bencénico con un grupo hidroxilo añadido.
Éteres: R-O-R
Mercaptanos: R-SH
Tioéteres: R-S-R
Tioácidos: R-COSH
Aldehidos: R-CHO
Cetonas: R-CO-R
Ácidos Carboxílicos: R-COOH
Sales: R-COOM (M de metal)
Ésteres: R-COO-R
Anhídridos: R-CO-O-OC-R
Aminas: R-NH2, R-NH-R, 2R-N-R
Carbohidratos tipo Aldosa: -CHOH-CHOH-CHO
Carbohidratos tipo Cetosa: -CHOH-CO-CH2OH
Compuestos organometálicos: R-M-R
Halogenuros de Metal-Alkilo: R-MX (también conocidos como Reactivos de Grignard)
¿Cómo citar? Contreras, V. & Del Moral, M. (s.f.). Ejemplo de Química Orgánica.Ejemplo de. Recuperado el 26 de Septiembre de 2023 de https://www.ejemplode.com/38-quimica/4509-ejemplo_de_quimica_organica.html
