Características De Los Electrolitos
Los electrolitos son soluciones acusas que puede conducir la electricidad. Esto sucede porque las sustancias disueltas se dividen en iones, que tienen carga eléctrica.
Cuando en un solvente químicamente neutro, se disuelve una sustancia que se disocia iónicamente, el líquido resultante resulta conductor de la electricidad, y tenemos un electrolito. Los electrolitos más comúnmente conocidos utilizan el agua como solvente. Bajo algunas condiciones también los gases pueden contener iones cargados eléctricamente, que les dan propiedades conductoras de la electricidad. A este estado de la materia se le llama plasma.
Las principales características de los electrolitos son:
- Están formados por un solvente que en condiciones normales, es eléctricamente aislante.
- Las sustancias que se disuelven (solutos), se disocian en iones cargados eléctricamente. Estas sustancias pueden ser ácidos, bases o sales.
- La solución resultante es conductora de la electricidad.
- Al pasar una corriente eléctrica los iones disueltos se polarizan y se dirigen hacia los electrodos que proporciona la corriente. Al polo positivo se le llama ánodo y al polo negativo cátodo.
- Los iones con carga negativa se les llama aniones.
- Los iones con carga positiva se les llama cationes.
- Al pasar corriente eléctrica, los cationes se dirigen al cátodo donde se neutralizan, mientras que los aniones se dirigen al ánodo.
Los electrolitos tienen múltiples usos en la química y en la industria. Se utilizan para obtener gases como sucede a disolver ácido sulfúrico en agua: al paso de la corriente se disocian las moléculas de agua, dando como resultado que en el cátodo se acumule hidrógeno y en el ánodo se acumule oxígeno.
Este mismo principio se utiliza para depositar otros elementos o sustancias ionizados sobre otros metales; así sucede, por ejemplo, con la solución de sulfato de cobre, la cual, al paso de la corriente eléctrica, deposita el cobre en el cátodo, mientras que en el ánodo se forma ácido sulfúrico y se desprende oxígeno. Otra aplicación de este principio es el baño de oro. En una solución de cloruro de oro se hace pasar corriente eléctrica, en la que la pieza que se desea dorar está conectada en el cátodo.
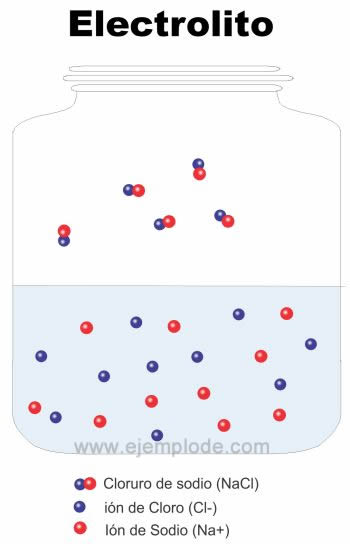
Los iones pueden ser elementales o radicales. Los iones elementales son aquellos formados por átomos de un solo elemento, como sucede al disolver cloruro de sodio en agua, desprendiéndose iones de sodio (Na+) y de cloro (Cl-). Los radicales son fracciones de moléculas compuestas por más de un elemento, como sucede en la disociación del hidróxido de sodio (sosa cáustica), que da como resultado iones de sodio (Na+) y radicales hidróxilo (OH-).
Los electrolitos también son muy importantes para la vida, pues las funciones de alimentación de las células requieren cargas eléctricas que permiten a las sustancias atravesar la membrana celular. Es por ello que los líquidos del cuerpo, especialmente la sangre, contienen elementos químicos disueltos, lo que le da ciertas características de acidez. Incluso el agua potable, el agua que necesitamos para vivir, no puede ser químicamente neutra, ya que no permitiría el transporte de sustancias alimenticias; por ello, en condiciones naturales el agua también es ligeramente ácida, ya que contiene disueltas electrolíticamente diversas sustancias, tales como aire, algunos minerales y algunas sales.
¿Cómo citar? Figueroa, D. & Del Moral, M. (s.f.). Características De Los Electrolitos.Ejemplo de. Recuperado el 26 de Septiembre de 2023 de https://www.ejemplode.com/38-quimica/3955-caracteristicas_de_los_electrolitos.html
