Ejemplo de Ley De Charles
La ley de los gases de Charles o Ley de la presión constante, es otra de las leyes de los gases, enunciada por Gay-Lussac, quien dio a conocer el trabajo de Jacques Charles, publicado alrededor de 20 años antes.
La ley de Charles predice el comportamiento de una masa de gas cuando la presión permanece constante y varían la temperatura y el volumen.
La ley de Charles se enuncia de la siguiente forma:
A presión constante, el volumen de un gas es directamente proporcional a la variación de su temperatura.
Presión constante: se refiere a que la presión que el gas ejerce sobre las paredes del recipiente no tendrá variación a lo largo de la experiencia.
Volumen: es el espacio ocupado que ocupa el gas, en general se considera un recipiente con paredes que no se deforman, y cuya tapa funciona a manera de émbolo.
Temperatura: es el aumento o pérdida de calor que sufre el gas durante la experimentación. Si aumenta la temperatura, aumenta el volumen. Si la temperatura disminuye, el volumen también disminuye.
Algebraicamente, la Ley de Charles se expresa con la siguiente fórmula:
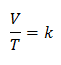
Donde:
V = volumen del gas
T = Temperatura del gas
k = constante de proporcionalidad para esa masa de gas.
Esto significa que para una determinada masa de gas, a presión constante, la relación entre el volumen y las variaciones de temperatura, siempre tendrá la misma relación de proporcionalidad, representada por la constante k:
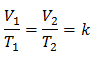
Por lo que una vez determinada la constante, podemos calcular cualquiera de los otros valores a partir de los demás datos conocidos:
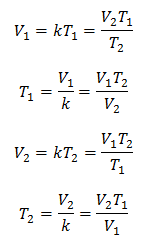
3 Ejemplos de la Ley de Charles aplicada a problemas:
Ejemplo 1: Calcular el nuevo volumen, si en un recipiente se encuentra una masa de gas que ocupa un volumen de 1.3 litros, a una temperatura de 280 K. Calcular el volumen al alcanzar una temperatura de 303 K.
V1 = 1.3 l.
T1 = 280 K
V2 = ?
T2 = 303 K
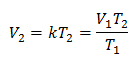
Sustituyendo valores:
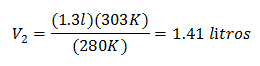
El nuevo volumen a 303 K es de 1.41 litros.
Ejemplo 2. Si tenemos un gas que a 10 grados centígrados ocupa 2.4 litros, calcular la temperatura final, si al terminar ocupa 2.15 litros.
V1 = 2.4 l
T1 = 10 °C = 283 K
V2 = 2.15 l
T2 = ?
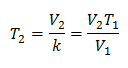
Sustituyendo valores:

La nueva temperatura es de 253 K, que es igual a -20° C.
Ejemplo 3. Tenemos un gas del que sabemos que su temperatura inicial es de 328 K, el volumen final es de 3.75 l, y su constante de relación es de 0.00885.
V1 = ?
T1 = 328 K
V2 = 3.75 l
T2 = ?
k = 0.00885
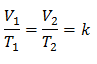
Sustituyendo valores:
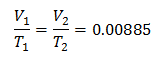
Para conocer el Volumen inicial:
![]()
El volumen inicial es de 2.90 l.
Para conocer la temperatura final:
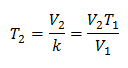
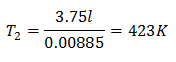
La temperatura final será del 423 K, lo que es igual a 150°C.
¿Cómo citar? Figueroa,V. & Del Moral, M. (s.f.). Ejemplo de Ley De Charles.Ejemplo de. Recuperado el 26 de Septiembre de 2023 de https://www.ejemplode.com/37-fisica/4223-ejemplo_de_ley_de_charles.html

Últimos 10 comentarios